“Μ����ΓΔΥα–‘»ή“ΚΚΆâA–‘»ή“Κ
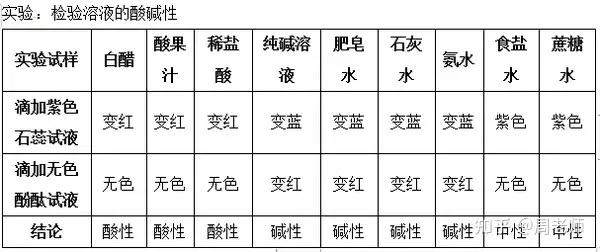
ΫY’™ΘΚ
(1)Ζ≤ «Ρή ΙΉœ…Ϊ ·»ο‘΅“ΚΉÉΦtΒΡ»ή“ΚΕΦ «Υα–‘»ή“ΚΘ§≤Δ«“‘™»ή“Κ≤ΜΡή Ιüo…ΪΖ”ΧΣ‘΅“ΚΉÉ…Ϊ;
(2)Ζ≤ «Ρή ΙΉœ…Ϊ ·»ο‘΅“ΚΉÉΥ{ΒΡ»ή“ΚΕΦ «âA–‘»ή“ΚΘ§≤Δ«“‘™»ή“ΚΡή Ιüo…ΪΖ”ΧΣ‘΅“ΚΉÉΦt;
(3)≤ΜΡή ΙΉœ…Ϊ ·»ο‘΅“ΚΉÉ…Ϊ���Θ§“≤≤ΜΡή Ιüo…ΪΖ”ΧΣ‘΅“ΚΉÉ…ΪΒΡ»ή“ΚΘ§Έ“²ÉΖQûι÷––‘»ή“Κ����ΓΘ
(4)»γΉœ…Ϊ ·»ο‘΅“ΚΦΑüo…ΪΖ”ΧΣΒ»Ρήôzρû»ή“ΚΥαâA–‘ΒΡ‘΅“ΚΘ§ΖQûιΥαâA÷Η Ψ³©����ΓΘ
ΉΔ“βΘΚΔΌΈ“²É”–ïrΚρΏÄ”ΟΥ{…ΪΜρΦt…Ϊ ·»ο‘΅Φà¹μôzρû»ή“ΚΒΡΥαâA–‘;
ΔΎΥα–‘»ή“ΚΡή ΙΥ{…Ϊ ·»ο‘΅ΦàΉÉΦtΘ§âA–‘»ή“ΚΡή ΙΦt…Ϊ ·»ο‘΅ΦàΉÉΥ{;
Δέ÷Μ”–Ω…»ή–‘ΒΡΥα–‘���ΓΔâA–‘ΈοΌ|≤≈Ρή Ι÷Η Ψ³©ΉÉ…ΪΘ§ΉÉ…ΪΒΡ «÷Η Ψ³©����Θ§Εχ≤Μ «‘™ΈοΌ|ΓΘ
2.»’≥Θ…ζΜν÷–≥Θ“äΒΡΥα–‘ΈοΌ|≈câA–‘ΈοΌ|
(1)Υα–‘ΈοΌ|ΘΚ…ΫιΪ���ΓΔôéΟ ���ΓΔΗΧιΌΓΔΈςΦt ΝΒ»;
(2)âA–‘ΈοΌ|ΘΚ≤η»~âA����ΓΔüüâAΒ»���ΓΘ
3.Ö^(q®±)Ζ÷Υα»ή“ΚΚΆΥα–‘»ή“ΚΓΔâA»ή“ΚΚΆâA–‘»ή“Κ
ΉΔ“βΘΚΥα»ή“Κ «÷ΗΥαΒΡΥ°»ή“Κ���Θ§Υα–‘»ή“Κ «÷ΗΡή ΙΉœ…Ϊ ·»ο‘΅“ΚΉÉΦtΒΡ»ή“Κ���Θ§“ρ¥ΥΥα»ή“Κ“ΜΕ® «Υα–‘»ή“ΚΘ§ΕχΥα–‘»ή“Κ≤Μ“ΜΕ® «Υα»ή“Κ;Ά§‰”���Θ§âA–‘»ή“Κ≤Μ“ΜΕ® «âA»ή“Κ����Θ§âA»ή“Κ“ΜΕ® «âA–‘»ή“Κ���ΓΘ
άΐ»γΘΚΝρΥαψ~���ΓΔ¬»Μ·δ@ΒΡΥ°»ή“Κο@Υα–‘Θ§Εχ≤Μ «Υα;ΦÉâA���ΓΔΖ ‘μΒΡΥ°»ή“Κο@âA–‘����Θ§ΒΪ≤Μ «âAΓΘ
4.―a≥δ÷ΣΉRΘΚΥα����ΓΔâAΓΔϊ}ΒΡΗ≈Ρν
(1)ΥαΘΚκäκxïr…ζ≥…ΒΡξ•κxΉ”»Ϊ≤Ω «öδκxΉ”ΒΡΜ·ΚœΈο���ΓΘ»γΘΚHCl����ΓΔHNO3���ΓΔH2SO4���ΓΔH2CO3Β»����ΓΘ
HCl==H++Cl-;H2SO4==2H++SO42-;
(2)âAΘΚκäκxïr…ζ≥…ΒΡξéκxΉ”»Ϊ≤Ω «öδ―θΗυκxΉ”ΒΡΜ·ΚœΈοΓΘ»γΘΚNaOH���ΓΔCa(OH)2Β»����ΓΘ
NaOH==Na++OH-;Ca(OH)2==Ca2++2OH-;
(3)ϊ}ΘΚκäκxïr…ζ≥…Ϋπ¨ΌκxΉ”(Μρδ@ΗυκxΉ”)ΚΆΥαΗυκxΉ”ΒΡΜ·ΚœΈοΓΘ»γΘΚNaCl����ΓΔNH4NO3Β»ΓΘ
NaCl==Na++Cl-;NH4NO3==NH4++NO3-;
Εΰ���ΓΔ»ή“ΚΒΡΥαâA–‘ΒΡèä»θ
1.ΥαâAΕ»ΘΚ”Ο¹μ±μ Ψ»ή“ΚΒΡΥα–‘ΜρâA–‘ΒΡèä»θ≥ΧΕ»����ΓΘ
2.pH‘΅Φà”Ο¹μΕ®ΝΩΒΡ€yΕ®»ή“ΚΒΡΥαâAΕ»���ΓΘ
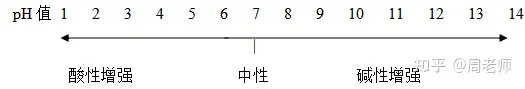
»ή“ΚΒΡpH÷Β≈cΥαâA–‘ξPœΒ:
pH=7���Θ§»ή“Κ≥ ÷––‘;pH<7Θ§»ή“Κ≥ Υα–‘���Θ§«“pH‘Ϋ–Γ����Θ§Υα–‘‘Ϋèä;pH>7Θ§»ή“Κ≥ âA–‘���Θ§«“
pH‘Ϋ¥σ����Θ§âA–‘‘Ϋèä���ΓΘ
3.pH‘΅ΦàΒΡ Ι”ΟΖΫΖ®:
”ΟΡzν^ΒΈΙή(Μρ≤ΘΝßΑτ)Α―¥ΐ€y‘΅“ΚΒΈ(ΜρΆΩ)‘ΎpH‘΅Φà…œ����Θ§»ΜΚσΑ―‘΅Φàο@ ΨΒΡν¹…Ϊ(ΑκΖ÷γäÉ»)≈c‰Υ€ ±»…ΪΩ®¨Π’’����Θ§‰Υ€ ±»…ΪΩ®…œœύΆ§ν¹…ΪΒΡpHΦ¥ûι‘™»ή“ΚΒΡpHΓΘ
ΉΔ“βΘΚ
(1)≤ΜΡή÷±Ϋ”Α―pH‘΅ΦàΫΰ»κ¥ΐ€y»ή“Κ÷–����Θ§“‘Οβéß»κκsΌ|Θ§Ά§ïrΏ@ΖN≤ΌΉςΩ…Ρή≈ίΒτpH‘΅Φà…œ
“Μ≤ΩΖ÷÷Η Ψ³©����Θ§“‘÷¬±»…ΪΑl(f®Γ)…ζί^¥σΒΡ’`≤ν;
(2)≤ΜΡήœ»”ΟΥ°¨ΔpH‘΅Φàùôùώ���Θ§‘ΌΏM––€y‘΅���Θ§“ρûιΥ°ùôùώΚσΒΡpH‘΅Φà¨Δ€yΕ®ΒΡ «œΓα¨Κσ»ή
“ΚΒΡpH����ΓΘ
(3)Έ“²É¨çρû ““Μ‰” Ι”ΟΒΡpH‘΅Φà «èVΖΚpH‘΅Φà����Θ§€y≥ωΒΡpH÷Β «1~14ΒΡ’ϊîΒ(sh®¥)ΓΘ
(4)ûιΝΥ±»ί^ΨΪ¥_ΒΡ€yΕ®»ή“ΚΒΡpH����Θ§Έ“²ÉΩ…“‘”ΟΨΪΟήpH‘΅ΦàΚΆΥαΕ»”΄(”÷ΖQpH”΄)¹μ€yΝΩΓΘ
»ΐ���ΓΔ»ή“ΚΥαâA–‘≈c…ζΟϋΜν³”ΒΡξPœΒ
1.»ΥΒΡσw“Κ”–“ΜΕ®ΒΡΥαâAΕ»���ΓΘ―Σ“ΚΓΔΫMΩ½ιg“ΚΚΆΦöΑϊÉ»“ΚΒΡΥαâAΕ»ΕΦΫ”Ϋϋ”Ύ÷––‘���Θ§Εχ«“ΉÉΜ·‰O–Γ;
2.ΈΗ“ΚΒΡpH‘Ύ0.9~1.5÷°ιg���Θ§‘ΎΏ@‰”ΒΡ≠h(hu®Δn)Ψ≥÷–ηF–ΦΕΦΩ…±Μ»ήΫβ���Θ§ΒΪΈΗ±Ψ…μÖsΡήΑ≤»ΜüoμΠΓΘ“ρûιΈΗάο”–“Μ¨”“’≥“ΚΤΝ’œ”���Θ§Υϋ «”…’≥“ΚΦöΑϊΚΆ…œΤΛΦöΑϊΖ÷ΟΎ≥ωΒΡ“ΜΖNΡzÉω†ν’≥“Κ����Θ§‘ΎΈΗ’≥ΡΛ±μΟφ‰΄≥…“Μ²Ä±ΘΉoΡΛ���Θ§”Ο¹μ±ΘΉoΈΗ���Θ§Ζά÷ΙΈΗΥα¨ΠΤδ±Ψ…μΒΡΗ·ΈgΦΑΈΗΒΑΑΉΟΗ¨ΠΈΗ±Ψ…μΒΡœϊΜ·Θ§ΏÄΡήΖά÷Ι¥÷≤ΎΒΡ ≥Έο¨ΠΈΗΒΡôC–Β–‘™p²ϊ����ΓΘ
3.¥σΕύîΒ(sh®¥)ΒΡόr(n®°ng)ΉςΈοΏm“Υ‘ΎΫ”Ϋϋ÷––‘(pH‘Ύ6.5~7.5÷°ιg)ΒΡΆΝ»ά÷–…ζιLΘ§‘ΎΗΡΝΦΥα–‘ΆΝ»άïr����Θ§Έ“²É“ΜΑψ « Ι”Ο λ ·Μ“¹μ’{Ιù(ji®Π)ΤδΥαâAΕ»ΓΘ
4.”ξΥ°“ΜΑψ≥ ¬‘Υα–‘(”…”ΎΩ’öβ÷–ΒΡΕΰ―θΜ·ΧΦ»ήΫβ‘Ύ”ξΥ°÷–)����Θ§»Υ²É“ΜΑψΑ―pH–Γ”Ύ5.6 ΒΡ”ξΥ°ΖQûιΥα”ξ����ΓΘ
§7.2 ≥Θ“äΒΡΥαΚΆâA
“Μ���ΓΔ≥Θ“äΒΡΥα
1.…ζΜν÷–≥Θ”ΟΒΡΥαΘΚΈΗ“Κ÷–Κ§”–ΒΡϊ}Υα(HCl)Θ§–νκä≥Ί÷–Κ§”–ΝρΥα(H2SO4)����Θ§Υα”ξ÷–Κ§”–ΒΡΝρΥαΦΑœθΥα(HNO3)Θ§ ≥¥Ή÷–Κ§”–ΒΡ¥ΉΥα(CH3COOHΜρHAc);ο΄Νœ÷–Ω…ΡήΚ§”–ΒΡΧΦΥα���ΓΔôéΟ ΥαΒ»���ΓΘ
2.ΥαΒΡΖ÷νêΘΚüo―θΥα(»γHCl)ΓΔΚ§―θΥα(HNO3����ΓΔH2SO4)Β»ΓΘ
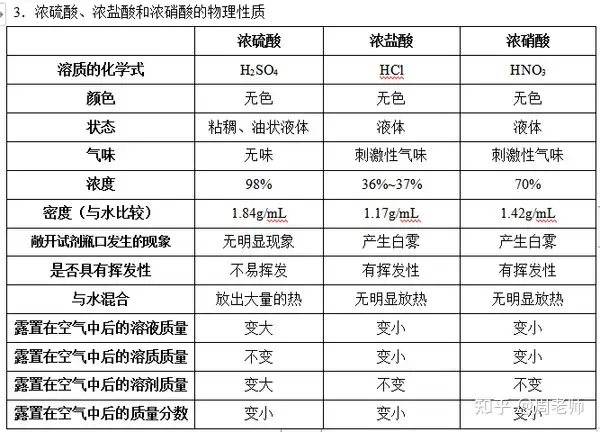
ΉΔ“βΘΚùβΝρΥαΨΏ”–“ΜΕ®ΒΡΧΊ–‘ΘΚ
(1)ΈϋΥ°–‘(Έοάμ–‘Ό|)”Ο”ΎöβσwΗ…‘ο���Θ§ΒΪ≥ΐNH3Β»âA–‘öβσw≥ΐΆβ[2NH3+ H2SO4== (NH4)2SO4]
(2)Ο™Υ°–‘(Μ·¨W–‘Ό|)——ΚΎΟφΑϋ¨çρû(ùβΝρΥα≈c’αΧ«Ζ¥ëΣ����Θ§ Ι÷°ΧΩΜ·ΓΘ)
(3)èä―θΜ·–‘���Θ§Η·Έg–‘——≈cΫπ¨ΌΑl(f®Γ)…ζΖ¥ëΣ���Θ§…ζ≥…ΒΡöβσw≤Μ…ζ≥…öδöβΕχ «Εΰ―θΜ·ΝρΓΘ
‘ΎΦ”üαΒΡ½lΦΰœ¬���Θ§Ρή≈c≈≈‘ΎöδΚσΟφΒΡΫπ¨Ό(»γCu)Ζ¥ëΣ���Θ§»γΘΚ
Cu+2H2SO4(ùβ)Γς==CuSO4+SO2↑+H2O
”÷»γΘ§άδΒΡùβΝρΥα≈cηFΜρδXΖ¥ëΣΚσ���Θ§Ρή…ζ≥…“Μ¨”÷¬ΟήΒΡ―θΜ·ΡΛ����Θ§Ήη÷ΙΖ¥ëΣΏM“Μ≤ΫΏM––����ΓΘ
(4)ùβΝρΥαΒΡœΓα¨ΘΚΥα»κΥ°Θ§―ΊΤς±Ύ���Θ§≤Μîύî΅Αη���ΓΘ
ùβΝρΥα»ή”ΎΥ°Ζ≈≥ω¥σΝΩΒΡΥ°���Θ§Ήψ“‘ ΙΥ°Ζ÷Ζ–ρvΘ§≤Δ«“Υ°ΒΡΟήΕ»–Γ”ΎùβΝρΥαΒΡΟήΕ»���ΓΘ»γΙϊΑ―Υ°ΒΙ»κùβΝρΥα÷–Θ§Υ°ΨΆïΰΗΓ‘ΎùβΝρΥα…œΟφ����Θ§»ήΫβïrΖ≈≥ω¥σΝΩΒΡüαΘ§÷¬ ΙΥ°Ζ–ρvΕχ ΙΝρΥα“ΚΒΈœρΥΡ÷ήοwûRΕχ‘λ≥… ¬Ι ����ΓΘ
(5)Α≤»Ϊ ¬Ι ΒΡΧéάμΘΚùβΝρΥαûRΒΫΤΛΡw…œΚσΘ§ Ήœ»―ΗΥΌ”ΟΡ®≤Φ¨ΔΤδ≤Ν Ο����Θ§»ΜΚσ”Ο¥σΝΩΥ°¦_œ¥Θ§ΉνΚσ”Ο3%~5%ΒΡNaHCO3ΆΩΖσ���ΓΘ
œΓΝρΥαûRΒΫΤΛΡw…œΚσ���Θ§ëΣ‘™ώR…œ¦_œ¥���Θ§“ρûικS÷χœΓΝρΥα÷–»ή³©ΒΡ’τΑl(f®Γ)Θ§“≤ïΰΉÉ≥…ùβΝρΥα����ΓΘ
4.ΥαΒΡΜ·¨W–‘Ό|
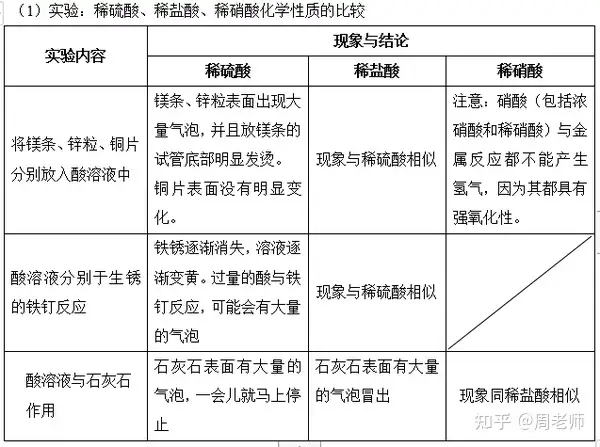
Ω²ΫYΘΚΥαΥυΨΏ”–ΒΡΙ≤Ά§ΧΊϋcΘΚ
Υα‘ΎΥ°»ή“Κ÷–ΕΦΡήκäκx≥ωöδκxΉ”Θ§“ρ¥ΥΥα»ή“ΚïΰΨΏ”–‘SΕύΙ≤Ά§ΒΡ–‘Ό|(ΥαΒΡΈε¥σΆ®–‘)ΘΚ
(1)Υα»ή“Κ≈cΥαâA÷Η Ψ³©ΒΡΖ¥ëΣ
A.Ήœ…Ϊ ·»ο‘΅“ΚΜρΥ{…Ϊ ·»ο‘΅Φà”ωΒΫΥα»ή“ΚΉÉΦt…Ϊ;
B.üo…ΪΖ”ΧΣ‘΅³©”ωΒΫΥα»ή“Κ≤ΜΉÉ…Ϊ���ΓΘ
Χα–―ΘΚΉœ…Ϊ ·»ο‘΅³©ΉÉ…Ϊ«ι¦rûιΘΚ“ΥαΦtâAΥ{”; «÷Η Ψ³©ΉÉ…Ϊ����Θ§ΕχΖ«¥ΐ€y»ή“Κ±Ψ…μΉÉ…Ϊ����ΓΘ
(2)Υα»ή“Κ≈cΡ≥–©Ϋπ¨ΌΖ¥ëΣ
Υα»ή“Κ+ (öδ«Α)Ϋπ¨Ό→ ϊ}»ή“Κ+ öδöβ
ΉΔ“βΘΚ
A.‘ΎΫπ¨ΌΜν³”–‘μ‰–ρ±μ÷–Θ§≈≈‘Ύöδ«ΑΟφΒΡΫπ¨ΌΡή÷Ο™Q≥ωΥα÷–ΒΡöδ���Θ§≈≈‘ΎöδΚσΟφΒΡΫπ¨Ό³t≤ΜΡή;
B.≈≈‘ΎΫπ¨ΌΜν³”–‘μ‰–ρ±μ‘Ϋ«ΑΟφΒΡΫπ¨Ό���Θ§Ζ¥ëΣ§F(xi®Λn)œσ‘Ϋ³ΓΝ“Θ§ΥΌΕ»‘ΫΩλ���Θ§»γMgΖ¥ëΣ”–Οςο@Ζ≈
üα§F(xi®Λn)œσ;
C.èä―θΜ·–‘Υα≈cΫπ¨ΌΖ¥ëΣΚσ����Θ§≤ΜΡή…ζ≥…öδöβΘ§Εχ «…ζ≥…Υ°���ΓΘ»γùβΝρΥα���ΓΔœθΥαΒ»èä―θΜ·–‘Υα;
D.‘™νêΖ¥ëΣ¨Ό”Ύ÷Ο™QΖ¥ëΣ
»γΘΚZn + 2HCl == ZnCl2+ H2↑;Fe + H2SO4== FeSO4 + H2↑
(3)Υα»ή“Κ≈cΡ≥–©Ϋπ¨Ό―θΜ·ΈοΖ¥ëΣ(Ϋπ¨Ό―θΜ·Έο”÷ΖQâA–‘―θΜ·Έο)
Υα»ή“Κ+ Ϋπ¨Ό―θΜ·Έο→ ϊ}»ή“Κ+ Υ°
ΉΔ“βΘΚ‘™Ζ¥ëΣΏ^≥Χ÷–Θ§Ϋπ¨Ό‘ΣΥΊΒΡΜ·ΚœÉr≤ΜΉÉ����Θ§Υα÷–ΒΡ‘≠Ή”àF≤ΜΉÉ
»γΘΚCuO + 2HCl == CuCl2+ H2O;Fe2O3+ 3H2SO4== Fe2(SO4)3+ 3H2O
ZnO + 2HNO3== Zn(NO3)2+H2O
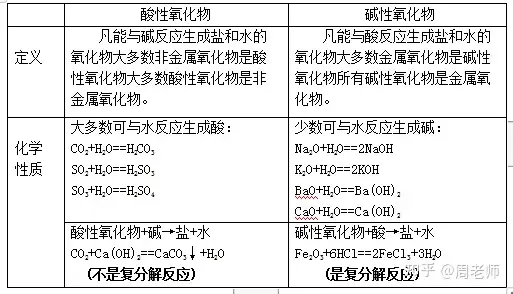
(4)Υα»ή“Κ≈câAΒΡΖ¥ëΣ(”÷ΖQûι÷–ΚΆΖ¥ëΣ)
Υα+âA→ϊ}+Υ°
(5)Υα»ή“Κ≈cΡ≥–©ϊ}Ζ¥ëΣ
Υα»ή“Κ+ ϊ}→ –¬Υα+ –¬ϊ}
ΉΔ“βΘΚA.Έ“²ÉΆ®≥Θ”ωΒΫΒΡϊ} «ΧΦΥαϊ}���Θ§“ρ¥ΥΫ^¥σ≤ΩΖ÷Ζ¥ëΣ «ΘΚ
Υα+ ΧΦΥαϊ}→ –¬ϊ}+ Υ°+ Εΰ―θΜ·ΧΦ
»γΘΚCaCO3+ 2HCl == CaCl2+ H2O + CO2↑;Na2CO3+ H2SO4== Na2SO4+ H2O + CO2↑;
K2CO3+ 2HNO3== 2KNO3+ H2O + CO2↑;
MgCO3+ CH3COOH == (CH3COO)2Mg + H2O + CO2↑;
B.Ρ≥–©ΧΊ βΒΡϊ}Ρή≈cΥαΖ¥ëΣ����Θ§…ζ≥…ΧΊ βΒΡ≥ΝΒμ
»γΘΚHCl + AgNO3== AgCl↓+ HNO3;BaCl2+ H2SO4== BaSO4↓+ 2HCl
―a≥δΘΚCl-ΦΑSO42-ΒΡôzρû
A.œρ¥ΐ€y»ή“Κ÷–Φ”»κAgNO3»ή“ΚΚσ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…���Θ§ΒΈ»κœΓœθΥα»ή“ΚΚσ���Θ§≥ΝΒμ≤Μœϊ ßΘ§³t»ή“Κ÷–Κ§”–Cl-Θ§»γΙϊ¦]”–≥ΝΒμΜρ’Ώ≥ΝΒμœϊ ß���Θ§³t≤ΜΚ§”–Cl-���ΓΘ
B.œρ¥ΐ€y»ή“Κ÷–Φ”»κBa(NO3)2»ή“ΚΚσ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…Θ§ΒΈ»κœΓœθΥα»ή“ΚΚσ���Θ§≥ΝΒμ≤Μœϊ ß����Θ§³t»ή“Κ÷–Κ§”–SO42-����Θ§»γΙϊ¦]”–≥ΝΒμΜρ’Ώ≥ΝΒμœϊ ßΘ§³t≤ΜΚ§”–SO42-����ΓΘ
Εΰ.≥Θ“äΒΡâA
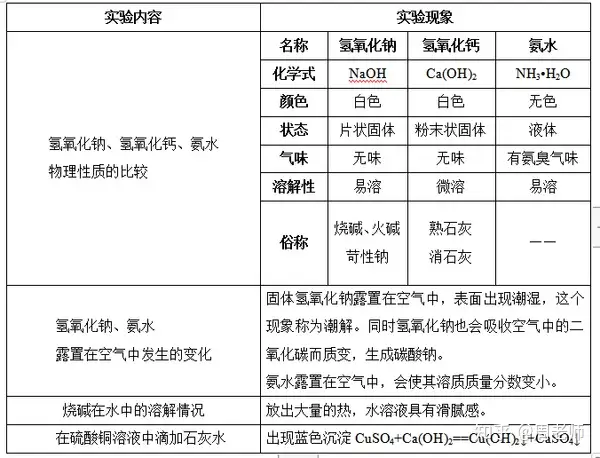
1.”–ξPâAΒΡ“Μ–©–‘Ό|±»ί^
üΐâAΨΏ”–èäΗ·Έg–‘Θ§öδ―θΜ·β}ΚΆΑ±Υ°“≤ΨΏ”–“ΜΕ®ΒΡΗ·Έg–‘���ΓΘ
öδ―θΜ·βc»ή“ΚΡήâρ≈cν^Αl(f®Γ)���ΓΔκuΒΑ«ε���ΓΔ÷≤Έο”ΆΒ»Αl(f®Γ)…ζΜ·¨WΖ¥ëΣΘ§»ήΫβΤδ÷–ΒΡΒΑΑΉΌ|����ΓΘ
2.âAΒΡΙ≤Ά§–‘Ό|
”…”ΎâAκäκxΚσΕΦΡή…ζ≥…OH-Θ§“ρ¥Υ“≤ΨΏ”–œύΆ§ΒΡ–‘Ό|(âAΒΡΥΡ¥σΆ®–‘)ΘΚ
»γΘΚNaOH == Na++ OH-;NH3•H2O == NH4++OH-;
(1)≈cΥαâA÷Η Ψ³©Ής”Ο
A.Ήœ…Ϊ ·»ο‘΅³©ΜρΦt…Ϊ ·»ο‘΅Φà”ωΒΫâA»ή“ΚΉÉΥ{;
B.üo…ΪΖ”ΧΣ”ωΒΫâA»ή“ΚΉÉΦt���ΓΘ
(2)≈cΡ≥–©Ζ«Ϋπ¨Ό―θΜ·ΈοΖ¥ëΣ(Ζ«Ϋπ¨Ό―θΜ·Έο”÷ΖQΥα–‘―θΜ·Έο)
âA»ή“Κ+ Ζ«Ϋπ¨Ό―θΜ·Έο→ ϊ}+ Υ°
»γΘΚ2NaOH + CO2== Na2CO3+ H2O;Ca(OH)2+ SO2== CaSO3↓+ H2O;
(3)≈cΥα»ή“ΚΒΡΖ¥ëΣ
âA+Υα→ϊ}+Υ°
(4)Ρή≈cΡ≥–©ϊ}Ζ¥ëΣ
âA»ή“Κ+ ϊ}»ή“Κ→ –¬ϊ}+ –¬âA
»γΘΚCuSO4+ 2NaOH == Na2SO4+ Cu(OH)2↓Ca(OH)2+Na2CO3==2NaOH+CaCO3↓
3.èΆΖ÷ΫβΖ¥ëΣΘΚ”–É…ΖNΜ·ΚœΈοœύΜΞΫΜ™Q≥…Ζ÷����Θ§…ζ≥…ΝμΆβÉ…ΖNΜ·ΚœΈοΒΡΖ¥ëΣ���ΓΘ
Ω…“‘”ΟΘΚAB + CD == AD + CB ±μ Ψ����ΓΘ
ΧΊϋcΘΚ(1)Ζ¥ëΣΈο���ΓΔ…ζ≥…ΈοΨυ÷Μ”–É…ΖNΜ·ΚœΈο;
(2)Αl(f®Γ)…ζΖ¥ëΣΒΡÉ…ΖNΜ·ΚœΈοœύΜΞΫΜ™Q≥…Ζ÷;
(3)Ης‘ΣΥΊΒΡΜ·ΚœÉr‘ΎΖ¥ëΣ«ΑΚσΨυ≤ΜΗΡΉÉΓΘ
ΉΔΘΚκy»ή–‘âA ήüα“ΉΖ÷Ϋβ(≤Μ¨Ό”ΎâAΒΡΆ®–‘)
§7.3 éΉΖN÷Ί“ΣΒΡϊ}
“Μ���ΓΔϊ}
1.ϊ}ΒΡΖ÷νêΘΚ“ά™ΰ(j®¥)ΫM≥…ϊ}ΒΡξ•κxΉ”ΚΆΥαΗυΒΡΖNνêΏM––Ζ÷νê
Ηυ™ΰ(j®¥)ξ•κxΉ”ΒΡ≤ΜΆ§���Θ§ϊ}Ω…“‘Ζ÷ûιβcϊ}����ΓΔβ¦ϊ}����ΓΔφVϊ}ΓΔηFϊ}����ΓΔδ@ϊ}Β»ΓΘ(¬»Μ·βcûιβcϊ})
Ηυ™ΰ(j®¥)ΥαΗυΒΡ≤ΜΆ§���Θ§ϊ}Ω…“‘Ζ÷ûιΝρΥαϊ}���ΓΔΧΦΥαϊ}ΓΔœθΥαϊ}����ΓΔϊ}Υαϊ}Β»ΓΘ(¬»Μ·βcûιϊ}Υαϊ})
2.Υα���ΓΔâA���ΓΔϊ}ΒΡ»ήΫβ–‘“é(gu®©)¬…ΘΚ
ΔΌΥαΕΦ»ή;ΔΎ»ήâA”–ΈεΈΜΘΚβ¦����ΓΔβc����ΓΔδ@ΓΔβ}����ΓΔδ^;Δέβ¦ϊ}ΓΔβcϊ}����ΓΔδ@ϊ}ΓΔœθΥαϊ}ΕΦΩ…»ή;Δήϊ}Υαϊ}÷Μ”–¬»Μ·ψy≤ΜΩ…»ή;ΔίΝρΥαϊ}÷Μ”–ΝρΥαδ^≤ΜΩ…»ή;ΔόΧΦΥαϊ}÷Μ»ήβ¦����ΓΔβcΓΔδ@����Θ§ Θœ¬ΕΦ≤Μ»ή���ΓΘ
ΉΔ“βΘΚAgCl����ΓΔBaSO4≤ΜÉH≤Μ»ή”ΎΥ°Θ§Εχ«“≤Μ»ή”ΎœΓœθΥα����ΓΘ
ΤΏΖN≥Θ“ä≥ΝΒμΘΚAgCl↓BaSO4↓Cu(OH)2↓F e(OH)3↓Mg(OH)2↓BaCO3↓CaCO3↓
3.ϊ}ΒΡΜ·¨W–‘Ό|ΘΚ
(1)ϊ} + Ϋπ¨Ό → –¬ϊ} + –¬Ϋπ¨Ό
‘ΎΫπ¨ΌΜν³”–‘μ‰–ρ±μ÷–Θ§≥ΐΖ«≥����ΘΜνùäΒΡΫπ¨ΌΆβΘ§≈≈‘Ύ«ΑΟφΒΡΫπ¨Ό“ΜΑψΩ…“‘¨ΔΈΜ”ΎΤδΚσΟφΒΡ���ΓΔ±»Υϋ≤ΜΜνùäΒΡΫπ¨ΌèΡΥϋ²ÉΒΡϊ}»ή“Κ÷–÷Ο™Q≥ω¹μ����Θ§»γΘΚ
Zn + CuSO4== ZnSO4 + Cu Cu + 2AgNO3== 2Ag + Cu(NO3)2
(2)Ρ≥–©ϊ}»ή“Κ‘Ύ“ΜΕ®½lΦΰœ¬Ρή≈cΥαΜρâAΑl(f®Γ)…ζèΆΖ÷ΫβΖ¥ëΣ
èΆΖ÷ΫβΖ¥ëΣΘΚ”…É…ΖNΜ·ΚœΈοΜΞœύΫΜ™Q≥…Ζ÷���Θ§…ζ≥…ΝμΆβÉ…ΖNΜ·ΚœΈοΒΡΖ¥ëΣ���ΓΘ
»γΘΚCuSO4+ Ca(OH)2 === Cu(OH)2↓ + CaSO4
Na2CO3+2HCl == 2NaCl+H2O+CO2↑
èΆΖ÷ΫβΖ¥ëΣΑl(f®Γ)…ζΒΡ½lΦΰΘΚ
a.”–≥ΝΒμ…ζ≥…;b.”–öβσwΖ≈≥ω;c.”–Υ°…ζ≥…;
d.»γΙϊ «¦]”–ΥαÖΔΦ”ΒΡΖ¥ëΣΘ§³tÉ…ΖNΖ¥ëΣΈο±ΊμöΕΦ»ή”ΎΥ°���ΓΘ
Εΰ����ΓΔéΉΖN≥Θ“äΒΡϊ}
1.¬»Μ·βc(NaCl)
‘ΎΉ‘»ΜΫγ÷–Ζ÷≤ΦΚήèVΖΚΘ§ΚΘΥ°÷–Κ§”–¥σΝΩ¬»Μ·βc���ΓΘ
2.ΧΦΥαβc(Na2CO3)
(1)ΥΉΟϊΘΚΦÉâA���ΓΔΧK¥ρ(2)ΦÉâA≤Μ «âAΘ§ «ϊ}(Υ°»ή“Κο@âA–‘)
(3)”ΟΆΨΘΚ≤ΘΝß���ΓΔ‘λΦà���ΓΔΦèΩ½ΚΆœ¥€λ³©ΒΡ…ζ°a(ch®Θn)Β»
(4)Na2CO3+ 2HCl === 2NaCl + CO2↑+ H2O
3.ΧΦΥαöδβc(NaHCO3)
(1)ΥΉΟϊΘΚ–ΓΧK¥ρ(2)”ΟΆΨΘΚ±Κ÷ΤΗβϋcΓΔ÷Έ·üΈΗΥαΏ^Εύ
(3)NaHCO3+ HCl === NaCl + CO2↑+ H2O
4.ΧΦΥαβ}(CaCO3)
(1)¥σάμ ·����ΓΔ ·Μ“ ·ΓΔγä»ι ·���ΓΔΊêöΛ����ΓΔ’δ÷ι����ΓΔΒΑöΛΓΔε¹†tΚΆΥ°âΊΒΡΥ°ΙΗΒΡ÷ς“Σ≥…Ζ÷
(2)”ΟΆΨΘΚΫ®÷ΰ≤ΡΝœ���ΓΔ―aβ}³©(3)CaCO3+2HCl===CaCl2+ CO2↑+H2O
―a≥δΘΚΧΦΥαϊ}(CO32-���ΓΔHCO3-)ΒΡôzρûΘΚ
A.œρ¥ΐ€y»ή“Κ÷–Φ”»κœΓHClΚσ”–öβ≈ί…ζ≥…Θ§¨Δ°a(ch®Θn)…ζΒΡöβσwΆ®»κ≥Έ«ε ·Μ“Υ°���Θ§»τ≥Έ«ε ·Μ“
Υ°ΉÉ€Üùα���Θ§³t»ή“Κ÷–Κ§”–CO32-;»τ≥Έ«ε ·Μ“Υ°üoΉÉΜ·Θ§³t»ή“Κ÷–≤ΜΚ§”–CO32-���ΓΘ
B.œρ¥ΐ€y»ή“Κ÷–Φ”»κBaCl2»ή“ΚΚσ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…���Θ§ΒΈ»κœΓHClΚσΘ§≥ΝΒμœϊ ß«“”–öβ≈ί…ζ
≥…���Θ§³t»ή“Κ÷–Κ§”–CO32-���ΓΘ
CaCO3+ 2HCl == CaCl2+ H2O + CO2↑
Na2CO3+ 2HCl == 2NaCl + H2O + CO2↑
NaHCO3+ HCl == NaCl + H2O + CO2↑
»ΐ���ΓΔΜ·¨WΖ Νœ
όr(n®°ng)ΉςΈοΒΡ…ζιL–η“ΣNΓΔP����ΓΔKΒ»†IπB(y®Θng)‘ΣΥΊΓΘΚ§”–Ώ@–©‘ΣΥΊΒΡΡ≥–©ΈοΌ|Ω…“‘ΉςûιΖ Νœ���ΓΘΆ®Ώ^Μ·¨WΦ”ΙΛ…ζ°a(ch®Θn)ΒΡΖ Νœ����Θ§ΖQΉςΜ·¨WΖ Νœ����ΓΘ
1ΓΔ≥Θ”ΟΒΡΖ ΝœΘΚ
Μ·¨WΖ ΝœΘΚΑ±öβ(NH3·H2O)����ΓΔΧΦΥαöδδ@(NH4HCO3)ΓΔΝρΥαβ¦(K2SO4)����ΓΔΝΉΒVΖέ[÷ς“Σ≥…Ζ÷ΝΉΥαβ}Ca3(PO4)2]���ΓΔΝρΥαδ@[(NH4)2SO4]����ΓΔΡρΥΊ[CO(NH2)2]ΓΔœθΥαβ¦(KNO3)����ΓΔΝΉΥαΕΰöδδ@(NH4H2PO4)ΓΘ
όr(n®°ng)Φ“Ζ ΝœΘΚ»γéΐΖ ���ΓΔ»ΥΦSΡρ���ΓΔΨGΖ Β»ΓΘ
2���ΓΔΒΣΖ Ής”ΟΘΚ¥ΌΏM÷≤Έο«o����ΓΔ»~…ζιLΟ· Δ���ΓΔ»~…ΪùβΨG(¥ΌΟγ)»±ΒΣΘΚ»~ϋS
β¦Ζ Ής”ΟΘΚ¥Ό ΙΉςΈο…ζιLΫΓâ―����ΓΔ«o½U¥÷”≤Θ§ΩΙΒΙΖϋ(â―Ε£)»±β¦ΘΚ»~ΦβΑl(f®Γ)ϋS���Θ§“ΉΒΙΖϋ
ΝΉΖ Ής”ΟΘΚ¥ΌΏM÷≤ΈοΗυœΒΑl(f®Γ)Ώ_����Θ§ΥκΝΘ‘ωΕύ����Θ§ο•ùM(¥ΏΙϊ)»±ΝΉΘΚ…ζιLΏtΨèΘ§°a(ch®Θn)ΝΩΫΒ
ΒΆ����Θ§ΗυœΒ≤ΜΑl(f®Γ)Ώ_
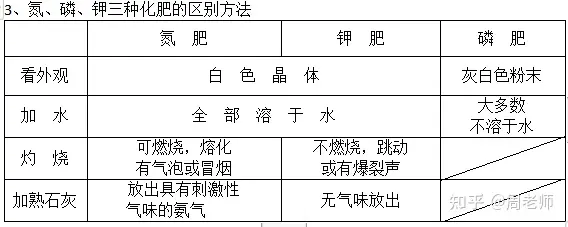
4ΓΔδ@ëB(t®Λi)ΒΣΖ ≈câAΜλΚœΦ”üα���Θ§ΕΦ”–Α±öβΖ≈≥ω:
(NH4)2SO4+ 2NaOH Γς==Na2SO4 + 2NH3↑+ 2H2O
NH4NO3+NaOH Γς==NaNO3+NH3↑+H2O
Α±öβ”–¥ΧΦΛ–‘öβΈΕ���Θ§Ρή Ι?ji®Π)ώùôΒΡΦt…Ϊ ·»ο‘΅ΦàΉÉΥ{Θ§Ώ@–©Ω…”Ο”Ύδ@ëB(t®Λi)ΒΣΖ ΒΡôzρû���ΓΘ
NH4+ΒΡôzρû:
‘΅³©ΘΚâA(NaOH���ΓΔCa(OH)2Β»)����ΓΔùώùôΒΡΦt…Ϊ ·»ο‘΅Φà
ΗΫΘΚÜΈΌ|���ΓΔ―θΜ·ΈοΓΔΥα���ΓΔâA����ΓΔϊ}ΒΡœύΜΞξPœΒ
(1)Ϋπ¨ΌÜΈΌ|+Υα---ϊ}+öδöβ(÷Ο™QΖ¥ëΣ)
1.δ\ΚΆœΓΝρΥαZn+H2SO4=ZnSO4+H2↑(Ήν≥Θ”Ο)
(¨çρû “÷ΤH2”ΟΒΡΫπ¨Ό”–Zn,Fe,Mg,Al���Θ§Υα”–œΓH2SO4ΚΆœΓHCl)
(2)Ϋπ¨ΌÜΈΌ|+ϊ}(»ή“Κ)---Νμ“ΜΖNΫπ¨Ό+Νμ“ΜΖNϊ}
2.ηFΚΆΝρΥαψ~»ή“ΚΖ¥ëΣΘΚFe+CuSO4=FeSO4+Cu
3.δXΚΆœθΥαψy»ή“ΚΖ¥ëΣΘΚAl+3AgNO3=Al(NO3)3+3Ag
(3)âA–‘―θΜ·Έο(Ϋπ¨Ό―θΜ·Έο)+Υα---ϊ}+Υ°
4.―θΜ·ηFΚΆœΓΝρΥαΖ¥ëΣΘΚFe2O3+3H2SO4=Fe2(SO4)3+3H2 O
5.―θΜ·β}ΚΆœΓϊ}ΥαΖ¥ëΣΘΚCaO+2HCl=CaCl2+H2 O
(4)Υα–‘―θΜ·Έο(Ζ«Ϋπ¨Ό―θΜ·Έο)+âA--------ϊ}+Υ°
6.ΩΝ–‘βc±©¬Ε‘ΎΩ’öβ÷–ΉÉΌ|ΘΚ2NaOH+CO2=Na2CO3+H2 O
7.œϊ ·Μ“Ζ≈‘ΎΩ’öβ÷–ΉÉΌ|ΘΚCa(OH)2+CO2=CaCO3↓+H2 O
(5)Υα+âA--------ϊ}+Υ°(÷–ΚΆΖ¥ëΣ)
8.ϊ}ΥαΚΆüΐâAΖ¥ëΣΘΚHCl+NaOH=NaCl+H2O
9.ϊ}ΥαΚΆöδ―θΜ·β}Ζ¥ëΣΘΚ2HCl+Ca(OH)2=CaCl2+2H2 O
10.öδ―θβcΚΆΝρΥαΖ¥ëΣΘΚ2NaOH + H2SO4==Na2SO4+2H2O
(6)Υα+ϊ}--------Νμ“ΜΖNΥα+Νμ“ΜΖNϊ}
11.¥σάμ ·≈cœΓϊ}ΥαΖ¥ëΣΘΚCaCO3+2HCl=CaCl2+H2 O+CO2↑(¨çρû “÷ΤCO2)
12.ΧΦΥαβc≈cœΓϊ}ΥαΖ¥ëΣ:Na2CO3 +2HCl=2NaCl+H2 O+CO2↑
13.ΝρΥαΚΆ¬»Μ·δ^»ή“ΚΖ¥ëΣΘΚH2SO4+BaCl2=BaSO4↓+2HCl
(7)âA+ϊ}---Νμ“ΜΖNâA+Νμ“ΜΖNϊ}
14.öδ―θΜ·β}≈cΧΦΥαβcΘΚCa(OH)2+Na2CO3=CaCO3↓+2NaOH
15.ΝρΥαψ~»ή“Κ≈cöδ―θΜ·δ^ΘΚCuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓
(8)ϊ}+ϊ}---É…ΖN–¬ϊ}
16.¬»Μ·βc»ή“ΚΚΆœθΥαψy»ή“ΚΘΚNaCl+AgNO3=AgCl↓+NaNO3
17.ΝρΥαβcΚΆ¬»Μ·δ^ΘΚNa2SO4+BaCl2=BaSO4↓+2NaCl
èΆΖ÷ΫβΖ¥ëΣ±Ίμö…ζ≥…≥ΝΒμ����Θ§öβσwΜρΥ°…ζ≥…≤≈ΡήΑl(f®Γ)…ζ���Θ§«“…ζ≥…ΈοΒΡ‘ΣΥΊΜ·ΚœÉr≤ΜΉÉ����ΓΘ
+1Ér:HClO;NaClO;Ca(ClO)2.
+5Ér:HClO3;KClO3.
+7Ér:HClO4;KClO4.
ΓΓΓΓ ög”≠ Ι”Ο ÷ôCΓΔΤΫΑεΒ»“Τ³”‘O²δ‘LÜ•÷–ΩΦΨW(w®Θng)����Θ§2024÷–ΩΦ“Μ¬Ζ≈ψΑιΆ§––ΘΓ>>ϋc™τ≤ιΩ¥
















